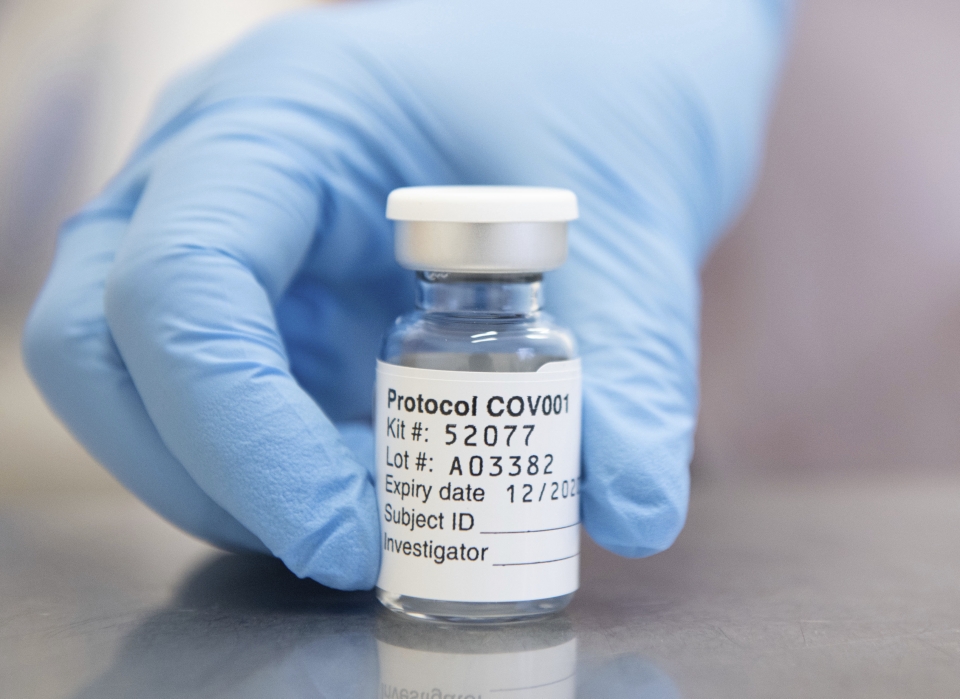
[뉴스토피아 고천주 기자]영국 옥스퍼드대와 글로벌제약사 아스트라제네카가 공동 개발한 신종 코로나바이러스 감염증(코로나19) 백신이 미국에서 내년 중반이 돼야 식품의약국(FDA) 승인을 받을 수 있을 것이라는 보도가 나왔다.
9일(현지시간) 로이터통신에 따르면 아스트라제네카 백신 개발을 총괄하는 애드리안 힐 제너연구소 소장은 "FDA가 임상시험이 끝나길 기다리면 내년 중반이 돼야 미국에서 백신을 구할 수 있을 것"이라고 밝혔다.
미국 NBC뉴스 공식 트위터 계정에 올라온 글에서 힐 소장은 “효과적이고 대규모로 사용 가능한 이 백신의 가치를 쉽게 보급하고 사용하기에는 너무 늦는다”며 "FDA가 내년 1월 입수할 수 있는 모든 자료를 포함해 이 백신에 관한 자료를 보길 바란다"며 신속한 승인을 촉구했다.
앞서 8일 뉴욕타임스에 따르면 아스트라제네카는 아직까지 미국에서 임상 3상 시험을 마치지 못했다며 "아스트라제네카 백신이 FDA의 신뢰를 잃고 있다"며 연내 승인이 불가능하다고 보도했다.
FDA 백신 승인을 위한 임상 시험 기준은 3만명인데, 이달 초까지 절반 정도밖에 채워지지 않았다는 것이다. 지난 9월 임상 시험 참가자에게서 부작용이 발생했음에도 FDA에 통보가 늦어져 임상 시험이 7주가량 중단됐기 때문이다.
지난달 23일 발표된 아스트라제네카의 임상3상 결과도 문제가 됐다. 당시 회사 측은 백신의 평균 예방 효과가 70%였다고 발표했는데, 뒤늦게 90%의 예방 효과를 보인 저용량 투약 방식이 연구진의 실수였다는 점을 공개했다.
이에 따라 당초 내년 초 FDA 승인을 받을 수 있을 거라 예상됐지만, 현재로선 여러 백신들 중에서 미국에 가장 늦게 승인을 받을 가능성이 커졌다. 내년 1분기부터 단계적으로 아스트라제네카 백신을 들여올 예정인 한국에도 영향을 미칠 가능성이 높아졌다.

